Puntos de vista
Actualización en diagnóstico y manejo de las demencias. Aportes prácticos en nuestro contexto
Updating the Diagnosis and Management of Dementia. Practical Contributions in our Context
Cómo citar este artículo:
Copyright: Esta revista provee acceso libre inmediato a su contenido bajo el principio de que hacer disponible gratuitamente investigación al publico apoya a un mayor intercambio de conocimiento global. Esto significa que se permite la copia y distribución de sus contenidos científicos por cualquier medio siempre que mantenga el reconocimiento de sus autores, no haga uso comercial de las obras y no se realicen modificaciones de ellas.

Recibido: 2011-10-28 07:43:35
Aprobado: 2011-12-05 10:22:01
Correspondencia: Ángel Julio Romero Cabrera. Hospital General Universitario Dr. Gustavo Alderegía Lima jromero@gal.sld.cu
RESUMEN
Con el objetivo de exponer el estado del arte sobre el diagnóstico y tratamiento de las demencias insistiendo en los últimos avances, y sugerir aportes prácticos para su manejo en este contexto, se brinda una panorámica acerca de la importancia de las demencias como problema de salud. Se plantean los elementos imprescindibles para el diagnóstico y abordaje de esta afección, que incluye el diagnóstico del deterioro cognitivo, sus variantes, el diagnóstico etiológico, el diagnóstico del síndrome demencial, la importancia de la valoración neuropsiquiátrica y las opciones del tratamiento. Se resalta la necesidad de la orientación adecuada de la familia y el cuidador.
Palabras clave: adulto mayor; demencia; enfermedad de Alzheimer
ABSTRACT
Key words: Aged; dementia; Alzheimer disease; intelligence tests; neuropsychological tests
INTRODUCCIÓN
La demencia o, de forma más apropiada, el síndrome demencial, se ha convertido en un problema de salud de índole mundial que afecta alrededor de 24 millones de personas en todo el planeta, con una incidencia de 4,6 millones de casos anualmente.1 Afecta no sólo al enfermo, sino también a su familia y a los cuidadores generando discapacidad y mala calidad de vida en el primero y mal funcionamiento y estrés en los segundos.
La demencia puede definirse como un síndrome clínico caracterizado por una variedad de síntomas y signos manifestados por dificultades en la memoria, trastornos en el lenguaje, cambios psicológicos y psiquiátricos, sobre todo conductuales, y deterioro en las actividades de la vida diaria.2 Como causa primaria de las demencias, la enfermedad de Alzheimer es una afección específica, que afecta alrededor de un 6 % de las personas mayores de 65 años, y su incidencia se incrementa con la edad, calculándose que afecta al 20 % de las personas de 80 años.3, 4 En Cuba, la encuesta del Grupo 10/66 encontró una prevalencia de demencia entre un 6,4 % y un 10,8 % según diferentes criterios de clasificación.5
Es una enfermedad costosa; el costo anual de su cuidado se calcula en el Reino Unido en 17 billones de libras esterlinas, más que la enfermedad cardiaca, cerebro vascular y el cáncer. El costo anual por paciente en los Estados Unidos se estima en 57 000 dólares, en Italia 64 000 dólares, en Suecia 24 000 dólares y en Canadá, 14 000.6
La demencia es una de las principales causas de discapacidad; cada año contribuye a esta con un 11,2 % aproximadamente, más alto que el ictus (9,5 %), los trastornos músculo esqueléticos (8,9 %), la enfermedad cardiaca (5 %) y el cáncer (2,4 %).7
Los pacientes con demencia no deben ser estigmatizados, ni enfrentados con pesimismo, tanto por parte del médico como por parte de sus familiares, pues si bien no existe una cura para esta afección, estas personas pueden vivir varios años (hasta 8 ó 9) lo que la hace una enfermedad crónica que requiere de medidas terapéuticas en el sentido de aliviar, rehabilitar, cuidar y mejorar la calidad de vida, por lo que el nihilismo terapéutico no está permitido.
En este estudio, el interés se centra en exponer el estado del arte sobre el diagnóstico y tratamiento de las demencias, insistiendo en los últimos avances, así como sugerir aportes prácticos para su manejo.
DESARROLLO
¿Cuáles son los pasos necesarios que debe dar el médico para el diagnóstico del síndrome demencial?
El diagnóstico de demencia solo debe ser realizado después de una evaluación integral, la cual debe incluir:
- Entrevista al paciente, familiares o cuidador.
- Examen físico general y por sistemas, profundizando en el examen neuropsiquiátrico. Al respecto se sugiere utilizar instrumentos evaluativos.
- Exámenes complementarios: Se indicarán los exámenes de laboratorio habituales y aquellos dirigidos a la confirmación de una causa secundaria cuando hay fuerte sospecha de ella.
- Establecer el diagnóstico diferencial.
Interrogatorio
Se debe confeccionar la historia médica individual y familiar insistiendo en los siguientes aspectos durante el interrogatorio:
- ¿Toma algún medicamento?
- ¿Cómo y cuándo comenzaron los problemas? ¿Los síntomas han progresado por pasos o empeoraron progresivamente? ¿Varían de un día a otro? ¿Qué tiempo han durado?
- El médico debe preguntar acerca de la habilidad para vivir solo; si paga cuentas, cocina, realiza tareas del hogar solo, realiza compras solo, realiza juegos que requieren habilidades, presta atención y entiende los programas de la televisión, libros, o revistas, sale a su vecindario, si maneja o utiliza el transporte público.
- Se debe evaluar el grado de dependencia para las actividades de la vida diaria (AVD).
¿Qué podemos encontrar?
Alteraciones frecuentes que pueden estar presentes en el paciente.
- Dificultad para aprender y recordar nueva información. Repetición de cosas dichas o hechas previamente. Olvido de conversaciones o citas, o del lugar en que puso las cosas.
- Manejo de tareas complejas. Problemas al ejecutar tareas que requieren varios pasos, por ejemplo, como cocinar.
- Capacidad de razonamiento. Dificultades al solucionar problemas diarios en el trabajo de la casa.
- Habilidad espacial y orientación. Dificultades al manejar o al encontrar el camino en lugares que le son familiares.
- Lenguaje. Problemas para encontrar las palabras y expresar lo que quiere decir.
- Conducta. Dificultades para prestar atención. Está más irritable o menos confiado que de costumbre.
Examen físico
Se debe insistir en los siguientes aspectos:
- Evaluación nutricional.
- Problemas visuales y auditivos.
- Determinar la presencia de nuevas condiciones, o deterioro de enfermedades crónicas pre- existentes (anemia, insuficiencia cardiaca, enfermedades respiratorias, del tracto urinario, digestivo y neurológico).
- Si se sospecha delirio el examen debe enfocarse también a detectar infecciones respiratorias y urinarias.
Instrumentos evaluativos
Estudios de psicogeriatría en Estados Unidos, Canadá y el Reino Unido han encontrado constantemente que el miniexamen del estado mental (Mini Mental State Examination - MMSE) es el instrumento o herramienta cognitiva más comúnmente usada. Sin embargo, la razón más frecuente para la pobre acogida de esta prueba por los clínicos, es el tiempo que toma llevarla a cabo. Por lo tanto, hay necesidad práctica de pruebas más cortas que retengan la sensibilidad y especificidad. Están disponibles otras herramientas, también de uso común, para la exploración del deterioro cognitivo. El valor de estos métodos es más difícil de establecer en analfabetos, presencia de disfasia y personas con pérdida sensorial. Han sido reportadas muchas diferencias en cuanto a su uso e interpretación.
El miniexamen del estado mental (MMSE)3, 8, 9 es un instrumento de evaluación de 30 puntos. Fue inicialmente desarrollado como una prueba de investigación para diferenciar desórdenes cognitivos orgánicos de los no orgánicos (por ejemplo, la esquizofrenia). Más recientemente se ha convertido en un método de evaluación, y para monitorizar la progresión de la demencia y el delirio. Toma 8 minutos (rango 4 – 21) ejecutarla en ancianos hospitalizados. Valores de 23 ó menos para aquellos con nivel educacional de secundaria y más, y de 25 ó menos para aquellos con nivel educacional más alto, son comúnmente indicadores de deterioro. Como la puntuación declina con la edad avanzada, otros autores han recomendado cortes más bajos como 20 ó menos para indicar deterioro cognitivo. Sin embargo, puntajes más bajos en ancianos pueden simplemente reflejar la prevalencia más alta en este grupo de edad.
La evaluación cognitiva de Montreal (The Montreal Cognitive Assessment - MOCA)10 es una prueba de 30 preguntas que toma aproximadamente 10 minutos completar. Fue publicada en el 2005 por un grupo de investigadores de la Universidad McGill. Evalúa diferentes tipos de habilidades cognitivas e incluye la orientación, memoria a corto plazo, funciones ejecutivas, habilidades del lenguaje, y habilidades visuoespaciales. Incluye la prueba de dibujo del reloj y una prueba de función ejecutiva conocida como huella o pista b.
En un rango de 0 a 30 con puntuación de 26 ó más, se considera normal. Los datos del estudio inicial señalaron 22,1 como puntaje en el deterioro cognitivo ligero y 16,2 en personas con enfermedad de Alzheimer. Al ser útil en pruebas para la función ejecutiva en personas con MMSE en 26 ó más, también puede predecir demencia en personas con déficit cognitivo ligero.
La prueba mental abreviada (AMT)11 es una escala corta de 10 ítems, usada para evaluar deterioro. Proviene de 10 preguntas escogidas, derivadas del Mental Test Score (índice fuera de 34). Requiere componentes intactos como la memoria a corto y a largo plazo, la atención y la orientación. Una puntuación por debajo de 8, sugiere un déficit cognitivo significante. Puede proveer rápidamente una evaluación de la severidad; comparada con la obtenida por largas pruebas, puede tener suficiente habilidad discriminatoria para detectar cambios en la cognición, asociados al delirio post operatorio. Toma aproximadamente 3 minutos aplicarlo en ancianos. Existe también una versión de 4 preguntas del AMT (el AMT4), referidas a la edad, fecha de nacimiento, lugar, y año, solamente. El resultado se correlaciona bien con la forma más larga del AMT.11
La exploración de 6 ítems (SIS) está compuesta por tres preguntas orientadoras (día, mes y año) y una tarea de recordar 3 ítems derivadas de MMSE. Por cada ítem se obtiene un punto. Un puntaje bajo significa deterioro cognitivo. Estudios recientes son partidarios de asumir un puntaje de 4 como corte para señalar el deterioro cognitivo.8,9
La prueba de deterioro cognitivo de 6 ítems (6 CIT) es también conocida como test corto de orientación, memoria y concentración. Está constituído por 6 item del Blessed mental status test (de 26 item inicialmente). Incluye uno de memoria, dos de cálculo y tres de preguntas de orientación. Los componentes han dado importancia cuando el puntaje conduce a un valor entre 0 y 28. Estos requerimientos matemáticos pueden hacer este test menos apropiado en sitios médicos concurridos.8,9
El test del dibujo del reloj (The Clock Drawing Test-CDT)12 es una prueba para determinar deterioro visuoespacial, praxia construccional y deterioro frontal. Se le pide primero al paciente que dibuje un círculo, y después los números, como si fuera la esfera de un reloj. La incapacidad para poner correctamente los números alrededor del círculo puede ser debido a un deterioro visuoespacial, falta de atención o déficit en planificación. Finalmente se pide dibujar las manecillas del reloj para representar una hora en específico. Las 11 y diez es típicamente usada, lo cual mide la función ejecutiva frontal. Existen versiones alternativas de esta prueba y en algunas de ellas el reloj es previamente dibujado, al menos 15 tipos diferentes de calificación han sido probados. Las opiniones están divididas sobre cuál método es el mejor. El más simple es la escala de tres puntos, uno para el dibujo correcto del círculo, uno para el espacio apropiado de los números, y otro punto para las manecillas en la hora correcta. Típicamente toma de 1 a 2 minutos ejecutarlo.12
Es una prueba relativamente independiente de influencias de lenguaje y factores socioculturales. Con respecto a los méritos de esta prueba para detectar cambios tempranos y ligeros en la cognición, las opiniones están divididas, por lo que es utilizado solo como una prueba de exploración. Como otras pruebas breves de evaluación, es pobre para distinguir diferentes subtipos de demencias. Aunque puede detectar deterioro cognitivo, no tiene beneficios en el diagnóstico y seguimiento del delirio. Los resultados no están significativamente influidos cuando hay solo depresión. La sensibilidad y especificidad son ambas de un 85 %.
El mini- Cog añade el test de recordar tres palabras al Clock Drawing Test (CDT), y de este modo mejora el test de memoria. Toma cerca de 3 minutos ejecutarlo. Los sujetos son clasificados como portadores de deterioro cognitivo si son incapaces de recordar alguna de las tres palabras después de ejecutar la prueba del reloj, o si ellos recuerdan 1 ó 2 palabras y dibujan un reloj incorrectamente (Ej. el círculo, los números o las manecillas están incorrectas), el resultado es que el deterioro cognitivo está ausente o no, pero no tiene valor para seguimiento en la progresión de la enfermedad o para determinar el índice de severidad.13
La evaluación de la cognición por el médico de cabecera, tiene semejanzas con el mini-cog y combina tareas de memoria (un nombre y dirección) con el CDT. Contiene también breves componentes para analizar la memoria reciente y la orientación. Adicionalmente tiene un corto cuestionario de información que es ejecutado en aquellos pacientes con puntuación intermedia en la primera parte. Se estima que toma 5-6 minutos aplicarlo.
Existe una considerable dificultad en comparar escalas cortas de evaluación cognitiva. La sensibilidad y especificidad de los resultados variarán según la población estudiada, el puntaje considerado como normal y al comparar con la prueba de oro adoptada. Las evaluaciones han sido ejecutadas en poblaciones selectas con alta prevalencia de demencias, más que en muestras escogidas al azar dentro de la población anciana. El SIS, el 6CIT y el Mini-Cog, pueden ser considerados como una alternativa suficientemente confiable en relación al MMSE. La opción de cuál se prefiere, puede estar en consonancia con el ambiente en el cual se aplica el test.
El SIS es fácil de aplicar cuando el paciente está en emergencia, o durante pases de visita. El 6CIT requiere matemáticas esenciales donde puede usarse calculadora o computadora, por lo que se prefiere aplicar durante visitas a pacientes en la comunidad. Sin embargo, el dominio cognitivo limitado de todos estos test, los hace propensos a perder las demencias no Alzheimer.14
Diversos estudios longitudinales han mostrado que la mayor parte de las personas con deterioro cognitivo tienen un riesgo elevado de desarrollar demencia con una incidencia mayor en el grupo afectado por deterioro cognitivo ligero (DCL). Aunque algunos datos sugieren que la reversión a la función cognitiva es de un 25-30 %, estudios recientes prospectivos han mostrado menor proporción en quienes vuelven a un estado cognitivo normal y aquellos que lo hacen no quedan exentos de desarrollar la enfermedad.
Diagnóstico diferencial
Debe contar con las siguientes condiciones médicas que pueden semejar o acompañarse de deterioro cognitivo: delirio, depresión, psicosis y deterioro cognitivo inducido por medicamentos.
Delirio:15
- Comienzo brusco.
- Nivel de conciencia reducido.
- Deterioro de la memoria.
- Desorientación.
- Aumento de la actividad psicomotora.
- Fluctúa durante el día con empeoramiento nocturno.
- Atención desordenada.
- Alucinaciones frecuentes (visuales y auditivas).
- Duración breve y potencialmente reversible.
- Generalmente la causa se identifica por el interrogatorio, examen físico y exámenes complementarios.
Depresión:16
- Quejas subjetivas más graves que resultados objetivos.
- Estado de ánimo depresivo.
- Sensación de culpa y miedo a equivocarse.
- Inseguridad frente a los demás.
- Inicio rápido, menos de 6 meses.
- Mejoran los trastornos cognitivos con antidepresivos.
- Insomnio, aunque tranquilo.
- Orientado, puede encontrar ayuda.
- Criterios DSM-IV.
Propuesta de actuación ante un adulto mayor con deterioro cognitivo
Establecer una consulta de deterioro cognitivo con un equipo multidisciplinario integrado por especialistas de Psiquiatría, Neurología, Geriatría, Radiología, Psicología y Trabajo social. Los pacientes acudirían remitidos por los Equipos Multidisciplinarios de Atención Gerontológica (EMAG) de las diferentes áreas de salud. Luego de la evaluación clínica por los especialistas, se les realizaría la evaluación neuropsicológica, el miniexamen del estado mental, MOCA, escala de depresión y alguna otra necesaria para establecer el diagnóstico positivo y diferencial.
Los pacientes serán nuevamente vistos en consulta con el fin de establecer diagnóstico y conducta terapéutica. Se le realizarán exámenes complementarios básicos y pruebas de imágenes. En algunos casos será necesario reevaluar a los pacientes para establecer el diagnóstico (por ejemplo: depresión y déficit cognitivo ligero).
Diagnóstico diferencial entre los subtipos de demencias primarias
Una vez establecido el diagnóstico del síndrome de demencia, ha de buscarse una etiología. Algunos datos de la anamnesis permitirán avanzar la sospecha de un proceso u otro (degenerativo, vascular, o relacionado con otras demencias secundarias). Igualmente, la exploración física neurológica habrá puesto de manifiesto patrones típicos de unas entidades u otras (normalidad en el Alzheimer, hallazgos focales o trastorno de la marcha en los procesos vasculares o parkinsonismo y trastorno de la marcha en la enfermedad por cuerpos de Lewy).17
Propuesta de evaluación diagnóstica
Para el diagnóstico de las demencias es necesario seguir una minuciosa metodología partiendo desde el motivo de consulta del paciente o las referencias familiares.
Una vez establecido que el examen clínico y la evaluación cognitiva han confirmado la presencia de demencia, corresponde establecer su etiología, mediante un adecuado diagnóstico diferencial.
Con frecuencia suele argumentarse que no es necesario profundizar demasiado en este aspecto, porque la mayoría de los síndromes demenciales son irreversibles y la diferenciación etiológica sólo tiene interés académico, beneficiando poco al paciente.
Es cierto que solo la anatomía patológica puede confirmar una enfermedad de Alzheimer (EA), pero también lo es que simples exámenes de laboratorio bastan para diagnosticar hipotiroidismo, una neurolúes, o una avitaminosis B12, todas ellas demencias tratables. Pasar por alto enfermedades como estas es de consecuencias ominosas para el paciente, y eventualmente de consecuencias médico legales para el médico.
No evaluar la posibilidad de una depresión hará que el paciente continúe con sus deterioro cognitivo y no reciba un tratamiento que podría mejorarlo.
Además, la EA ya no es farmacológicamente intratable. El surgimiento reciente de anticolinesterásicos centrales de efecto cognitivo reconocido, hacen que se deba precisar el diagnóstico antes de indicarlas, ya que no se ha probado que estas drogas actúen en otras formas de demencia cortical. Por ello, es fundamental el diagnóstico diferencial aún en el caso particular de estas formas de demencia, por lo que resulta importante establecer una clasificación.
Tipos básicos y clasificación de las demencias
Tipos básicos de demencias:
Según el predominio cerebral de la lesión:
- Cortical
- Subcortical
- Global
- Focal
Según el síntoma dominante inicial:
- Alteración de la memoria
- Alteración del comportamiento y la conducta
- Alteración del lenguaje
- Otros síntomas: alteraciones motoras, sensoriales complejas, etc.
Las demencias corticales se caracterizan por el deterioro de funciones que dependen del procesado neocortical asociativo.
El término demencia subcortical designa el deterioro cognitivo que aparece en las enfermedades de las regiones subcorticales cerebrales, pudiendo deberse tanto a una alteración en los núcleos grises neuronales (estriado, tálamo, núcleos del tronco, cerebelo), como en la sustancia blanca subcortical que conecta los distintos centros cerebrales. El término subcortical es relativamente inapropiado, ya que casi siempre existe una disminución cortical acompañante. Los síntomas más característicos son: bradipsiquia, apatía, amnesia y ausencia de síntomas corticales.
Entre las demencias degenerativas primarias corticales, pueden citarse la enfermedad de Alzheimer, la enfermedad por cuerpos de Lewy, las demencias frontotemporales, y otras formas infrecuentes (esclerosis hipocámpica, demencia con gránulos argirófilos, etc.).
La enfermedad de Alzheimer se caracteriza por un curso crónico progresivo con tres grupos de síntomas primarios:2
- Síntomas de disfunción cognitiva: pérdida de memoria, dificultades en el lenguaje y disfunción ejecutiva que se manifiesta con la pérdida de la capacidad de planificar y coordinar tareas intelectuales de nivel superior.
- Síntomas psiquiátricos y conductuales: depresión, alucinaciones, agitación, agresividad, conducta sexual desinhibida, etc.
- Dificultades para realizar las actividades de vida diaria, que progresan desde las instrumentales (manejar, hacer compras) hasta las básicas (vestirse y comer).
- Estos síntomas progresan desde ligera pérdida de memoria hasta formas muy severas de demencia durante varios años.
La demencia por cuerpos de Lewy se caracteriza por un deterioro del funcionamiento diario con un buen funcionamiento de la memoria en los inicios de la enfermedad. Otras características son: cognición fluctuante (especialmente la atención y el estado de alerta), alucinaciones visuales y síntomas de síndrome parkinsoniano que suceden a la aparición del déficit mental (en esto se diferencia de la demencia de la enfermedad de Parkinson, en la que los síntomas parkinsonianos preceden a la demencia).18
Los trastornos del lenguaje y de la conducta son los hallazgos fundamentales de la demencia frontotemporal con preservación relativa de la memoria, lo que la diferencia de la enfermedad de Alzheimer.19 Son manifestaciones comunes la conducta social inapropiada y el embotamiento afectivo. Entre los trastornos del lenguaje se encuentran la pérdida de comprensión y el conocimiento del objeto (demencia semántica), así como el lenguaje no fluente y balbuceante (afasia no fluente progresiva).
Entre las principales causas de demencias primarias, se encuentran las demencias vasculares que responden a la siguiente clasificación:
- Demencia multiinfartos.
- Demencia por infarto estratégico.
- Demencia por enfermedad de pequeños vasos: Enfermedad de Binswanger; estado lacunar; angiopatía amiloidea con hemorragias; CADASIL (Cerebral Autosomal Dominant Arteriopathy with Subcortical Infarts and Leukoencephalopathy).
- Otras formas: Vasculitis, síndrome de Sneddon.
- Demencia por isquemia- hipóxica: Infartos incompletos de sustancia blanca; infartos de zona frontera.
- Demencia por hemorragias: Hematomas cerebrales; hematoma subcortical crónico; hemorragia subaracnoidea.
Los criterios para el diagnóstico de la demencia vascular (DSM-IV-TR) incluyen declinación de las funciones sociales u ocupacionales producto de múltiples déficits cognitivos. Los pacientes deben tener deterioro de la memoria, y uno ó más de los siguientes trastornos: afasia, agnosia, trastorno disejecutivo. También deben tener una combinación de los siguientes síntomas y signos en ausencia de delirio: trastornos de la marcha, debilidad de una extremidad, parálisis pseudobulbar, exageración de los reflejos y respuesta extensora plantar. Los signos deben estar presentes en el contexto de evidencias imagenológicas (en imágenes de resonancia magnética) que demuestren enfermedad cerebrovascular.20
Como se ha reflejado en las manifestaciones clínicas ya expuestas de las demencias degenerativas primarias, se resalta la importancia de un examen neurológico completo en la búsqueda de signos que permitan el diagnóstico diferencial entre ellas.
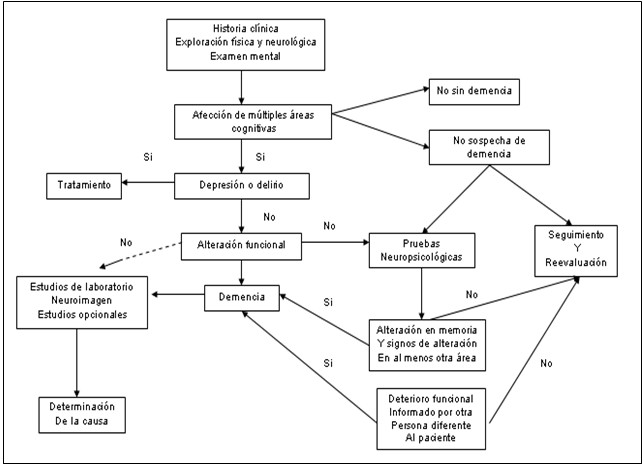
El siguiente algoritmo ilustra los pasos a seguir por el médico para encausar el diagnóstico de las demencias.
Avances de la imagenología en el diagnóstico de las demencias
La evaluación de un paciente con demencia incluye una combinación de herramientas diagnósticas, incluidas la historia y el examen físico, las pruebas del estado mental, un detallado examen neurológico, exámenes comunes de laboratorio y estudios de imágenes estructurales del cerebro, como la tomografía computarizada y las imágenes por resonancia magnética. Numerosos estudios han encontrado que la enfermedad de Alzheimer y otras enfermedades neurodegenerativas pueden producir alteraciones significativas en el metabolismo cerebral, las cuales son detectables con tomografía por emisión de positrones (PET), incluso en los estadios tempranos de la enfermedad.21-23
Los exámenes imagenológicos tienen extraordinaria importancia para el diagnóstico de las demencias, incluso, en algunos casos permiten establecerlo de manera definitiva, para determinar causas reversibles como los tumores o la hidrocefalia normotensiva, para hacer diagnóstico diferencial con otras situaciones clínicas que pudieran simularla, como la depresión y el delirio, y para medir el progreso de la enfermedad.
La imagenología cerebral puede ser de dos tipos: estructural y funcional. Desde el punto de vista estructural puede explorarse el cerebro mediante imágenes de resonancia magnética (RM) o con tomografía computarizada (TC). La RM define mejor la anatomía del cerebro y resulta muy útil en la detección de la pérdida de células cerebrales y en el diagnóstico de los tumores. La TC es útil para la detección de accidentes cerebrovasculares, infecciones del cerebro, traumatismos, hematomas, atrofia cerebral e hidrocefalia.
En la enfermedad de Alzheimer, los principales hallazgos tomográficos y por RM son:24
- Atrofia cerebral (hipocampo y corteza). En la RM se demuestran cambios tempranos en el hipocampo y la corteza entorrinal.25
- Ensanchamiento de surcos, fundamentalmente, en lóbulos temporal y parietal.
- Agrandamiento ventricular.
- Atrofia del cuerpo calloso.
- Cambios ligeros a moderados en la sustancia blanca (leucoaraiosis).
- La medición de la tasa de atrofia cerebral total en la RM se asocia fuertemente al deterioro cognitivo ligero y a la demencia y, en los pacientes no dementes incrementa el riesgo de progresión a la demencia.26
La demencia por cuerpos de Lewy se asocia con atrofia difusa pero sin un patrón característico en las imágenes de RM.27
En cuanto a la imagenología funcional, se utilizan dos tipos de estudios: la resonancia magnética funcional (RMF) que mide el metabolismo cerebral de la glucosa y el oxígeno, y la neuroimagenología molecular con sus dos variantes: la tomografía por emisión de positrones (PET) y la tomografía computarizada por emisión de fotones simples (SPET). Estos dos últimos estudios pueden detectar los depósitos amiloides, característicos de la enfermedad de Alzheimer.28
Los exámenes neuroimagenológicos han revolucionado el estudio estructural, pero no están asequibles para todos los pacientes. Por un lado tienen un alto costo, y por otro son de gran valor para descartar algunas causas, lo que hace que su empleo sea controversial.
Propuesta de exámenes imagenológicos a indicar en nuestro contexto
En nuestro hospital no contamos con estudios funcionales, por lo que los estudios a indicar serían la TC y la RM. Se recomienda que a todo paciente con síntomas y signos demenciales debe garantizársele un estudio imagenológico con la alta tecnología disponible (TAC o resonancia) independientemente de su edad, en busca de causas reversibles de su deterioro mental.
La TC es la prueba generalmente más disponible y menos costosa, y para la cual se han establecido los siguientes criterios de indicación:
- Deterioro cognitivo de un mes de evolución o menos.
- Historia de trauma: una semana antes del deterioro cognitivo.
- Cambios cognitivos rápidos (48 horas).
- Historia de: enfermedad cerebrovascular, convulsiones, defectos del campo visual, cefaleas, incontinencia urinaria, trastornos de la marcha.
Avances en el tratamiento de las demencias (terapia psicoconductual)
El tratamiento farmacológico con inhibidores de la acetilcolinesterasa y memantina (un antagonista de los neurorreceptores) ha aportado poco al curso natural de la enfermedad de Alzheimer y otras demencias. Otras opciones terapéuticas han mostrado mayor utilidad para alcanzar metas de mayor relevancia para estos pacientes, como son:
- Evitar o demorar la institucionalización.
- Preservar las actividades de vida diaria y las funciones cognitivas como leer, escribir, sostener conversaciones, y disfrutar de la televisión, la radio y la música.
- Mejorar la calidad de vida del paciente y sus cuidadores.
- Evitar los efectos adversos de los medicamentos y la hospitalización.
La enfermedad de Alzheimer constituye en la actualidad la demencia más frecuente a nivel mundial. En Cuba se comporta de la misma forma, con tendencia a seguir incrementándose, tanto por el aumento de la población anciana, como porque no existe un tratamiento que prevea, detenga o cure esta compleja enfermedad, tanto en su génesis como en sus manifestaciones.
Si bien en el presente existen diferentes fármacos que tratan de mejorar las alteraciones de la memoria y con ello las diferentes funciones cognitivas, el éxito hasta el presente es muy pobre y solo quedan como una luz que ilumina un largo camino a transitar por la neuropsicofarmacología, para llegar a obtener fármacos lo suficientemente eficaces. Esta situación ha motivado la búsqueda de formas de tratamiento que, sin el uso de fármacos, mejoren las funciones instrumentales de la vida diaria para influir positivamente en la calidad de vida del enfermo, cuidador y familia en general.
El tratamiento no farmacológico de los trastornos cognitivos29 es, sin lugar a dudas, la estrategia fundamental hasta el presente. No es más que el conjunto de estrategias rehabilitadoras de carácter terapéutico de las capacidades cognitivas, para mejorar o estabilizar las funciones instrumentales básicas de la vida diaria (AVD); tiene como objetivo conseguir la mayor calidad de vida del enfermo, cuidador y su familia, ya que ha de rehabilitar, restituir déficits, actuando sobre las funciones afectadas, para mantener, por ejemplo, la memoria, la orientación y el cálculo, entre otras funciones, con el fin de reincorporar al paciente a una vida familiar, social, activa y útil. Además de estas estrategias terapéuticas, se debe brindar atención a los trastornos de conducta, y en tal sentido, mostrar a la familia y cuidador una orientación práctica encaminada a disminuir o eliminar estos trastornos sin el uso de fármacos, teniendo en cuenta las causas que están determinando la afectación de esta esfera. Los principales problemas que se presentan son las alteraciones del sueño, el vagabundeo, los trastornos de la alimentación, las conductas sexuales inapropiadas, las preguntas repetitivas, reacciones catastróficas durante el baño, la agitación, las incontinencias, etc. De fallar, se utilizarían los psicofármacos como una alternativa de segunda línea.
Propuesta de afrontamiento de las demencias desde la perspectiva del cuidador
El profesional que atienda este tipo de trastornos, debe ser capaz de brindar una adecuada orientación a los familiares encargados de la custodia del enfermo, para ello, se recomienda lo siguiente:30
- Brindar información detallada a la familia sobre las características, evolución y principales complicaciones de la enfermedad.
- Brindar solidaridad.
- Lograr la participación activa y plena de toda la familia en el proceso de rehabilitación.
Las distintas afectaciones que provoca la enfermedad, exigen que una persona se encargue de cuidar y velar por el bien del paciente. Surge así el cuidador (con frecuencia una de las hijas de alrededor de 50 años de edad), quien, aunque reciba el apoyo de otras personas, adquiere la responsabilidad mayor, y se ve afectado por los siguientes motivos:
- Contrae una gran carga física y psíquica, pues se responsabiliza de la vida del enfermo: medicación, higiene, alimentación, y cuidados en general.
- Va perdiendo paulatinamente su independencia porque el enfermo cada vez le absorbe más.
- Se desatiende a sí mismo: no toma el tiempo libre necesario para su ocio, abandona sus aficiones, etc.
- Acaba paralizando durante años su proyecto vital.
Los aspectos mencionados pueden causar importantes problemas psicológicos en el cuidador principal, que frecuentemente tienen las siguientes manifestaciones:
- Agresividad constante contra los demás porque siguen su vida, porque son capaces de ser felices a pesar del problema que hay en la familia.
- Gran tensión contra los cuidadores auxiliares, porque consideran que todo lo hacen mal, no saben mover al enfermo, no le han dado a la hora adecuada el medicamento, los alimentos, etc.
- Aislamiento progresivo, y tendencia a encerrarse en sí mismo.
Por todo esto, el cuidador auxiliar conjuntamente con el resto de la familia, debe buscar soluciones viables para resolver tal problema, obligando al cuidador principal a que tome mayor tiempo de ocio, cubriendo esas horas con otro miembro de la familia o con asistente domiciliaria por cuidadores profesionales. El cuidador debe incrementar su socialización, buscar la ayuda especializada para recibir tratamiento adecuado a la situación real, ya sea debido a problemas físicos y/o psíquicos.
Por ello, es recomendable que el cuidador adquiera información de todo lo relacionado con la enfermedad de Alzheimer y su evolución, a fin de poder entender adecuadamente al enfermo y tomar las conductas adecuadas a las diferentes situaciones; la familia, sin dejarse agobiar por lo que sucederá y viviendo el presente, debe PLANEAR el futuro de su enfermo y el de la propia familia; y lo más importante, no puede descuidar su autoestima: debe por sí mismo.31
Algunas actitudes positivas, que deben caracterizar al cuidador, son las siguientes:
- Descansar cada día.
- Evitar las drogas para animarse.
- Hacer todo lo necesario para conservar su propia salud, buscando la ayuda profesional necesaria.
- No aislarse, mantener una adecuada interacción social con el resto de la familia, amigos, etc.
- Mantener alguna actividad que siempre le provoque placer. Por ejemplo: ir al cine, leer, ver la televisión, etc.
- La risa, el amor, la alegría, son fundamentales para su bienestar.
- Tener un tiempo semanal de descanso.
Llegada la etapa final de la enfermedad, y con ella la muerte del enfermo, esta debe afrontarse con firmeza. La muerte del ser querido es siempre un acontecimiento trascendental en la vida del cuidador; no por ser esperada, es menos trágica, dando lugar a sentimientos de tristeza y vacío. Con la muerte del enfermo comienza el “duelo”, durante el cual el cuidador debe ir “distanciándose adrede” de los sentimientos de tristeza, de culpa, depresivos, etc. mientras va restableciéndose en su libertad personal debe entonces el cuidador asumir actitudes positivas como son:
- Buscar nuevas ilusiones y afectos que lo lleven a dar cariño y atención a los demás: hijos, esposo, nieto, etc.
- Reemprender tareas que fueron abandonadas: estudio, trabajo, etc.
- Potencializar la recreación, el ejercicio físico, la alimentación adecuada, etc.
En definitiva, después de la muerte del enfermo, el cuidador ha de comenzar una vida diferente, en la que el tiempo pasado debe quedar como experiencia, y enfrentar el presente potencializando la confianza en sí mismo.
CONCLUSIONES
La demencia es un problema complejo pero abordable, y el personal profesional sanitario debe decir no al nihilismo diagnóstico y terapéutico en relación con las personas que acuden a las instituciones de salud con deterioro cognitivo. La detección precoz de este deterioro debe estar en la mira de la evaluación de toda persona mayor que consulte a un médico de atención primaria, aunque su diagnóstico definitivo requiera muchas veces de la valoración por un equipo multidisciplinario y su atención requiera de niveles según las etapas de la evolución de la enfermedad. Es necesario resaltar la necesidad de tratar no sólo al paciente, sino también al cuidador, en el cual deben crearse habilidades y actitudes positivas para enfrentar con éxito el manejo de estos enfermos.
REFERENCIAS BIBLIOGRÁFICAS
- Ferri CP, Prince M, Brayne C, Brodaty H, Fratiglioni L, Ganguly M, et al. Global prevalence of dementia: a Delphi consensus study. Lancet. 2005;366(9503):2112-17 [Buscar en Google Scholar]
- Burns A, Iliffe S. Alzheimer s disease. BMJ. 2009;338:b158 [Buscar en Google Scholar]
- Young J, Meagher D, Maclullich A. Cognitive assessment of older people. BMJ. 2011;343:d504 [Buscar en Google Scholar]
- National Institute for Health and Clinical Excellence. Dementia: A NICE- SCIE Guideline on supporting people with dementia and their carers in health and social care. Leicester (UK): British Psychological Society; 2007 [Buscar en Google Scholar]
- Llibre Rodríguez J, Valhuerdi A, Sánchez II, Reyna C, Guerra MA, Copeland JR, et al. The prevalence, correlates and impact of dementia in Cuba. A 10/66 Group Population-Based Survey. Neuroepidemiology. 2008;31(4):243-51 [Buscar en Google Scholar]
- Burns A, Iliffe S. Dementia. BMJ. 2009;338:b75 [Buscar en Google Scholar]
- Downs M, Bowers B. Caring for people with dementia. BMJ. 2008;336(7638):225-6 [Buscar en Google Scholar]
- Woodford HJ, George J. Cognitive assessment in the elderly: a review of clinical methods. QJM. 2007;100(8):469-84 [Buscar en Google Scholar]
- Ismail Z, Rajji TK, Shulman KI. Brief cognitive screening instruments: an update. Int J Geriatr Psychiatry. 2010;25(2):111-20 [Buscar en Google Scholar]
- Rossetti HC, Lacritz LH, Cullum CM, Weiner MF. Normative data for the Montreal Cognitive Assessment (MoCA) in a population-based sample. Neurology. 2011;77(13):1272-5 [Buscar en Google Scholar]
- Schofield I, Stott DJ, Tolson D, McFadyen A, Monaghan J, Nelson D. Screening for cognitive impairment in older people attending accident and emergency using the 4-item Abbreviated Mental Test. Eur J Emerg Med. 2010;17(6):340-2 [Buscar en Google Scholar]
- Parsey CM, Schmitter-Edgecombe M. Quantitative and qualitative analyses of the clock drawing test in mild cognitive impairment and Alzheimer disease: evaluation of a modified scoring system. J Geriatr Psychiatry Neurol. 2011;24(2):108-18 [Buscar en Google Scholar]
- McCarten JR, Anderson P, Kuskowski MA, McPherson SE, Borson S. Screening for cognitive impairment in an elderly veteran population: acceptability and results using different versions of the Mini-Cog. J Am Geriatr Soc. 2011;59(2):309-13 [Buscar en Google Scholar]
- Brodaty H, Pond D, Kemp NM, et al. The GPCOG: a new screening test for dementia designed for general practice. J Am Geriatr Soc. 2002;50(3):530-4 [Buscar en Google Scholar]
- National Institute for Health and Clinical Excellence. Delirium: diagnosis, prevention and management [monografía en Internet]. London (UK): National Clinical Guideline Centre; Acute and Chronic Conditions at The Royal College of Physicians; 2009 [citado 2 Dic 2011]. Disponible en: http://www.nice.org.uk/nicemedia/live/11874/48522/48522.pdf [Buscar en Google Scholar]
- Alexopoulos GS. Depression in the elderly. Lancet. 2005;365(9475):1961-70 [Buscar en Google Scholar]
- González Rodríguez VM, Marín Ibáñez A, Mateos González A, Sánchez Vázquez R. Diagnóstico sindrómico y etiológico. En: Guía de Buena Práctica Clínica en Alzheimer y otras demencias. 2da ed. Madrid : IM&C; 2009: p. 67-90 [Buscar en Google Scholar]
- Mollenhauer B, Försti H, Deuschle G, Storch A, Oertel W, Trenkwalder C. Lewy body and Parkinsonian dementia: common, but often misdiagnosed conditions. Dtsch Arztebl Int. 2010;107(39):684-91 [Buscar en Google Scholar]
- Cardarelli R, Kertesz A, Knebl JA. Frontotemporal dementia: a review for primary care physicians. Am Fam Physician. 2010;82(11):1372-7 [Buscar en Google Scholar]
- Reilly J, Rodríguez A, Lamy M, Neils-Strunjas J. Cognition, language, and clinical pathological features of Non-Alzheimer s dementias: An overview. J Commun Disord. 2010;43(5):438-52 [Buscar en Google Scholar]
- Silverman DHS, Small GW, Chang CY, Lu CS, Kung de Aburto MA, Chen W, et al. Positron Emission Tomography in Evaluation of Dementia. Regional Brain Metabolism and Long-term Outcome. JAMA. 2001;286(17):2120-2127 [Buscar en Google Scholar]
- Drugs for Alzheimer s Disease. Therapeutics Letter [revista en Internet]. 2005 [citado 19 Sep 2011];(56):[aprox. 7p]. Disponible en: http://www.ti.ubc.ca/newsletter/drugs-alzheimers-disease [Buscar en Google Scholar]
- Fernández de Larrinoa PP. Medición clínica de los trastornos psiquiátricos y del comportamiento en las demencias. Informaciones Psiquiátricas [revista en Internet]. 2003 [citado 5 Dic 2011];(172):[aprox. 12p]. Disponible en: http://www.revistahospitalarias.org/info_2003/02_172_08.htm [Buscar en Google Scholar]
- O Brien OT. Role of imaging techniques in the diagnosis of dementia. Brit J Radiol. 2007;80(2):S71-7 [Buscar en Google Scholar]
- Den Heijer T, van der Lijn F, Koudstaal PJ, Hofman A, van der Lugt A, Krestin GP, et al. A 10-year follow-up of hippocampal volume on magnetic resonance imaging in early dementia and cognitive decline. Brain. 2010;133(Pt 4):1163-72 [Buscar en Google Scholar]
- Sluimer JD, Bouwman FH, Vrenken H, Blankenstein MA, Barkhof F, van der Flier WM, et al. Whole-brain atrophy rate and cognitive decline: longitudinal MR study of memory clinics patients. Neurobiol Aging. 2010;31(5):758-64 [Buscar en Google Scholar]
- Tartaglia MC, Rosen HJ, Miller BL. Neuroimaging in dementia. Neurotherapeutics. 2011;8(1):82-92 [Buscar en Google Scholar]
- Rabinovici GD, Jagust WJ. Amyloid imaging in aging and dementia: testing the amyloid hypothesis in vivo. Behav Neurol. 2009;21(1):117-28 [Buscar en Google Scholar]
- Haro I. Abordajes no farmacológicos de las alteraciones del comportamiento en los pacientes con demencias. Informaciones Psiquiátricas [revista en Internet]. 2003 [citado 5 Dic 2011];(172):[aprox. 2p]. Disponible en: http://www.revistahospitalarias.org/info_2003/02_172_05.htm [Buscar en Google Scholar]
- Leturia Arrazola FJ, Yanguas Lezuán JJ, Arriola Manchola E, Uriarte Méndez A. La valoración de las personas mayores: evaluar para conocer, conocer para intervenir. Madrid: Cáritas; 2001 [Buscar en Google Scholar]
- Cordero Jiménez JR, García Cordero S, Fernández López O, Cañedo Santana L. Manual básico para el tratamiento de la enfermedad de Alzheimer. Medisur [revista en Internet]. 2005 [citado 5 Dic 2011];3 Suppl 1:[aprox. 20p]. Disponible en: http://www.medisur.sld.cu/index.php/medisur/article/view/96 [Buscar en Google Scholar]
Enlaces refback
- No hay ningún enlace refback.
FINLAY EN: 








FINLAY CERTIFICADA POR:

Esta revista "no aplica" cargos por publicación en ninguna etapa del proceso editorial.
Dirección postal: Calle 51A y Avenida 5 de Septiembre Cienfuegos, Cuba Código postal: 55100.
http://www.revfinlay.sld.cu
Telefono: +53 43 516602. Telefax: +53 43 517733.
amgiraldoni@infomed.sld.cu
ISSN: 2221-2434
RNPS: 5129